Aktuelle Konzepte der palliativen Systemtherapie bei Urothelkarzinom
Überblick:
- Alt-(bewährte) Chemotherapie
- Neuere Therapien (ICI)
- Neues (ADC, FGFR)
- Fazit
Alt-(bewährte) Chemotherapie
Therapiekonzept:
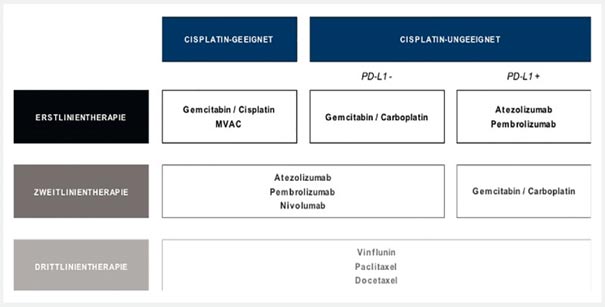
Quelle: Grunewald et al. (2020): Systemtherapie beim metastasierten Urothelkarzinom − Aktueller Stand und was kommt nach den Checkpointinhibitoren? Aktuelle Urol 2020; 51(04): 371-376
MVAC: Metastasiertes Setting: Ansprechrate MVAC: 72%, MÜZ: 12 -16 Monate
Gemcitabin/Cisplatin ungeeignet wenn: ECOG-Performance-Status ≥ 2, Krea < 60ml/min, Hörverlust ≥ Grad 2, Neuropathie ≥ Grad 2, NYHA ≥ 2
Carboplatin-Kombi: schlechte Wirksamkeit (Ansprechrate 30-40%, Mittlere Überlebenszeit (MÜZ) 8-9 Monate)
-> aktuelle S3-Leitlinie: Cisplatin in aufgeteilten Dosen wenn ECOG 0-1, GFR 40-60ml/min und keine weiteren Komorbiditäten, ggf. Monotherapie mit Gemcitabin
Neuere Therapien (ICI)
Immuncheck-Inhibitoren
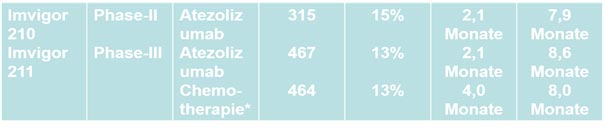
Atezolizumb: Ansprechrate 24%/ MÜZ 15,4 Monate
Pembrolizumab: Ansprechrate 24%/ MÜZ 11,5 Monate
(EMA seit 06/2018: NUR nicht Cisplatin-fähig und positiven PD-L1-Status)
Erstlinienerhaltungstherapie:
Avelumab (ICI)
- JAVE-LIN Bladder 100 (Phase-III Studie)
- Pat. nach Platin-basierter Therapie und 4-10 Wochen Rezidivfreiheit
Avelumab alle 2 Wochen: Gesamtpopulation MÜZ: 21,4 vs.14,3 Monate
versus
Best-Supportive-Care: PD-L1 pos. MÜZ: 17,1 vs.14,3 Monate
Zweitlinientherapie nach Platinhaltiger 1.-Therapie:

Pembrolizumab

Atezolizumab
Nivolumab

*Chemotherapie: Paclitaxel, Docetaxel oder Vinflunin
Synergismen?:
- ICI Ansprechrate max. 25%, kostenintensiv, lebensbedrohlicher immunvermittelter Nebenwirkungen
- Synergismen: Kombinationen aus klassischer Chemotherapie und Immuncheckpoint-Inhibition
- Ziel: verbesserte Erkennung und Eliminierung von Tumorzellen durch z.B. Induktion eines immunogenen Zelltods, positive Beeinflussung immunsuppressives Tumormilieu
- Erste Daten der IMvigor130-Studie:
- Vorteil der Kombinationsbehandlung gegenüber der alleinigen Chemotherapie hinsichtlich progressionsfreies Überleben (HR 0,82; 95% CI 0,70 – 0,96).
- Daten hinsichtlich des Gesamtüberlebens sowie weiterer Endpunkte stehen noch aus.
Zweitlinientherapie bei Platinungeeigneten PD-L1 positiver Patienten:
Expertenkonsens S3-Leitlinie: Kombi- oder Monotherapie
Aber: keine Empfehlung Therapieregime auf Grund fehlender Daten
ICI: keine Daten zur Wirksamkeit alternativer ICI
Drittlinientherapie:
Bisher keine explizite Empfehlung S3-Leitlinie: a.e. Vinflunin (Phase-III-Studie und kürzliche Zulassung)
ggf. Taxane
Mit welcher Wirksamkeit der Chemotherapie nach vorangegangener Immuntherapie zu rechnen ist, ist bisher unklar
Neues (ADC, FGFR)
Neues: Antikörper-Wirkstoff-Konjugate (ADC)
-
Insbesondere ICI vorbehandelte Patienten:
- ADC‘s: Enfortumab-Vedotin: Phase-III-Studie

NW: Häufigkeit und Schweregrad sowie therapiebedingte Todesfälle in beiden Gruppen vergleichbar
Häufiger: Enfortumab-Vedotin-Gruppe: Hautausschläge (44% vs. 10%) und periphere Polyneuropathien (46% vs. 30%)
FDA Ende 2019: Zulassung (Phase-II) bei Pat. mit Vorbehandlung Platin oder ICI (EMA Phase-III: Zulassung beantragt)
Neues: FGFR-Inhibitoren
-
FGFR-Inhibitoren
- Bislang keine publizierten Phase-III-Studie
- Aber: Phase-II-Studie 2019:
Erdafitinib-Zulassung durch FDA bei Patienten mit FGFR-Alterationen (Ansprechrate 40%, unabhängig von Anzahl Vortherapien, in mit ICI vorbehandelten Patienten stieg die Ansprechrate sogar auf 59%. MÜZ: 13,8 Monaten
Folge: Ergebnisse bleiben abzuwarten
Fazit:
Wachsende Kenntnis führt zu einer immer größer werdenden Zahl neuartiger Therapieansätze.
Insbesondere ADC und FGFR-Inhibitoren zeigten in bisherigen Untersuchungen sehr vielversprechende Ergebnisse.
Der Goldstandard des metastasierten Urothelkarzinoms stellt die Cisplatin-haltige Kombinations-Chemotherapie mit Erweiterung um PD-L1-Inhibitoren sowohl in der Erst- als auch in der Zweitlinie dar.
V.a. eine Kombination dieser beiden Regime als auch die Analyse ihrer optimalen Sequenz stellen aus heutiger Sicht wichtige Schwerpunkte zur Weiterentwicklung der Therapiemöglichkeiten im metastasierten Urothelkarzinom dar. In diesem Zusammenhang sollte man gerade auch dem Nebenwirkungsmanagement zukünftig eine große Bedeutung zukommen lassen.
Quellen:
Grunewald et al. (2020): Systemtherapie beim metastasierten Urothelkarzinom − Aktueller Stand und was kommt nach den Checkpointinhibitoren? Aktuelle Urol 2020; 51(04): 371-376
Niegisch (2021): Aktuelle Konzepte der palliativen Systemtherapie bei Urothelkarzinom Uroforum 6/2021: 30-34